你是否有這樣的疑問(wèn)�����,新購入的培養基�����,如何進(jìn)行技術(shù)性驗收來(lái)保證我們日常檢測的結果�?
答案是:根據GB4789.28-2013《食品安全國家標準 食品微生物學(xué)檢驗 培養基和試劑的質(zhì)量要求》來(lái)對培養基和試劑進(jìn)行驗收�����。該標準涉及到非常多的培養基和試劑類(lèi)別��,今天先給大家介紹一下固體培養基的性能測試方法�。
固體培養基的性能測試方法主要有兩種:半定量和定量方法���,其中����,定量測試方法在GB4789.28新標準的征求意見(jiàn)稿中成為了主要測試方法�,這次我們以平板計數瓊脂PCA為例�,為大家介紹非選擇性固體培養基性能測試方法的操作及注意事項�。
一���、定量測試方法
1�、操作步驟
1.1?根據培養基名稱(chēng)查附錄D���,獲得質(zhì)控菌株��、質(zhì)控指標和評定標準的相關(guān)信息����;
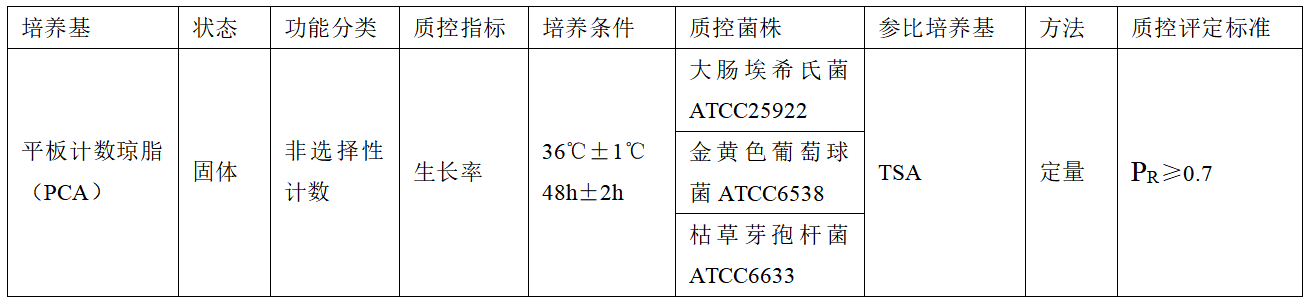
1.2 將質(zhì)控菌株接種到對應的非選擇性肉湯中培養過(guò)夜�����;
1.3?將菌懸液濃度調整到每平板接種水平為20 CFU~200 CFU��;
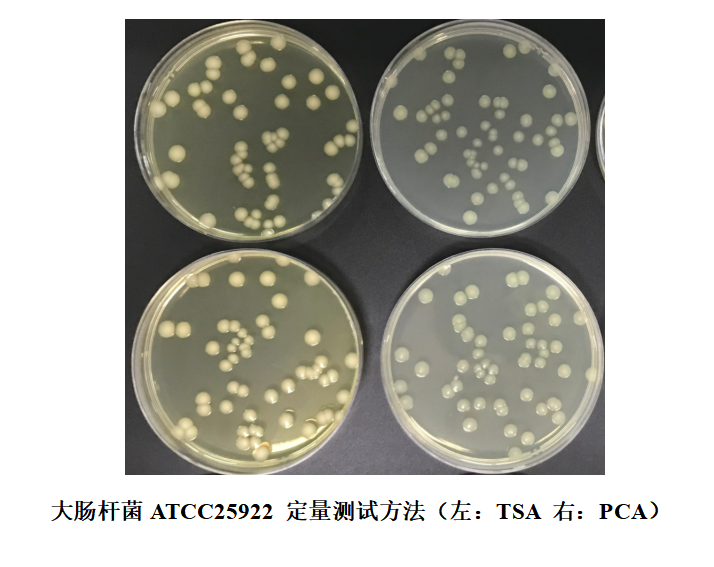
1.4 準備待測培養基平板���,將菌液涂布于待測培養基上����,同時(shí)涂布參比培養基①�����;(也可用傾注法或螺旋涂布法操作)
1.5 培養后����,計算參比培養基���、待測培養基上的菌落數�,計算生長(cháng)率②����,再與附錄D評定標準進(jìn)行對比判斷���。
?
注:①參比培養基:一般細菌采用TSA����,霉菌和酵母采用沙氏葡萄糖瓊脂�,對營(yíng)養有特殊要求的微生物采用適合其生長(cháng)的不含抑菌劑或抗生素的培養基���。
②生長(cháng)率PR:待測培養基平板上得到的菌落總數除以參比培養基平板上獲得的菌落總數得出的數值���。
2�、注意事項
在整個(gè)操作過(guò)程中���,步驟1.3菌懸液濃度調整為難點(diǎn)�,今天將分享一下菌懸液調整的方法:
2.1 培養后的新鮮菌液可先估計濃度��,如:常見(jiàn)的大腸埃希氏菌和金黃色葡萄球菌培養后原始菌液濃度可達到1*10^8CFU/mL以上��,枯草芽孢桿菌培養后可達到1*10^6CFU/mL以上���;
2.2 再根據所需菌懸液進(jìn)行梯度稀釋?zhuān)♂寱r(shí)可以采用10倍梯度稀釋法���。
新鮮菌液濃度估算方法:因每個(gè)實(shí)驗室的菌株活性和選擇的復活的培養基等不同�����,原始濃度會(huì )存在一些差異�����,建議先做菌濃度的預估實(shí)驗����。如常見(jiàn)的大腸埃希氏菌ATCC25922接種到BHI過(guò)夜培養后菌液濃度約為10^8CFU/mL�,對菌液進(jìn)行梯度稀釋后����,選擇10-6?�、10-7兩個(gè)稀釋度進(jìn)行計數�,通過(guò)計算結果可得出新鮮菌液的濃度�。以此數據作為該菌的原始濃度值�����。
二��、半定量測試方法
1����、操作步驟
1.1 查附錄E�����,獲得質(zhì)控菌株�����、質(zhì)控指標和評定標準的相關(guān)信息�����;
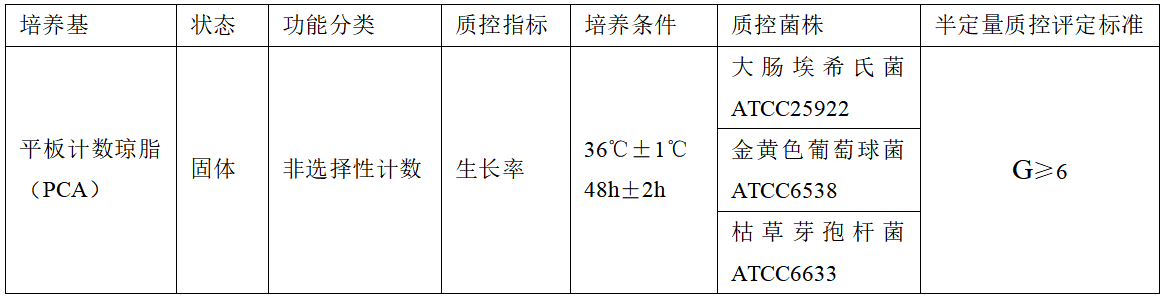
1.2 將質(zhì)控菌株接種到對應的非選擇性肉湯中培養過(guò)夜��;
1.3 用1μL接種環(huán)進(jìn)行平板劃線(xiàn)(如下圖所示)
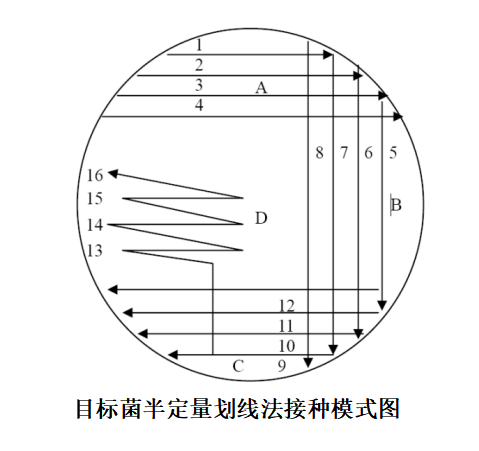
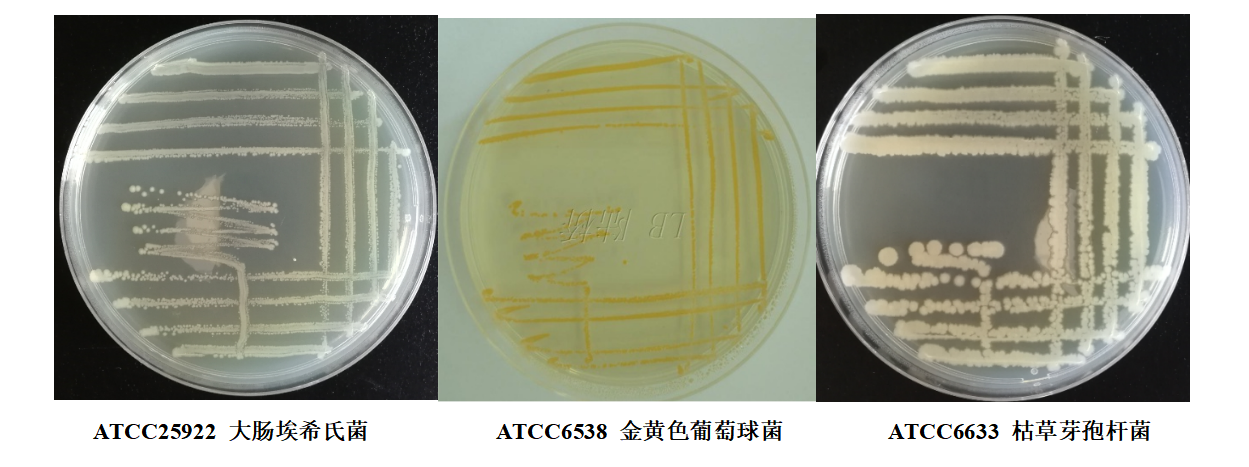
1.4 培養后�����,評價(jià)菌落的形狀�����、大小和生長(cháng)密度��,并計算生長(cháng)指數G�����。
2���、注意事項
使用1微升接種環(huán)(購買(mǎi)成品接種環(huán))����,自己制作的接種環(huán)無(wú)法保證準確的接種量����。
接種前菌液適度混勻�����,避免產(chǎn)生大量氣泡���,影響接種量��。
接種環(huán)浸入培養基液面下1cm左右�����,沾一滿(mǎn)環(huán)接種物���,避免沾取表層氣泡�����。
接種環(huán)與瓊脂平板表面角度適宜�����,一般為20°-30°�����。
劃線(xiàn)時(shí)力度與速度適宜�,前后均勻并且連續��。
可制作16條線(xiàn)模板置于平板底部�,便于操作�����。
每個(gè)菌種接種2個(gè)平板���,取平均值�。
測試片的質(zhì)控方法
在新發(fā)布的GB4789.2-2022《食品安全國家標準 食品微生物學(xué)檢驗 菌落總數測定》中��,新增了測試片方法�����,在使用測試片時(shí)���,應如何對其進(jìn)行技術(shù)驗收呢�����?
微生物測試片是一種特殊的培養基�����,它是以紙片��、冷水可凝膠或無(wú)紡布等作為培養基的載體�,用來(lái)檢測食品中的微生物���,考慮到其形式的特殊性�,建議采用定量測試方法��。
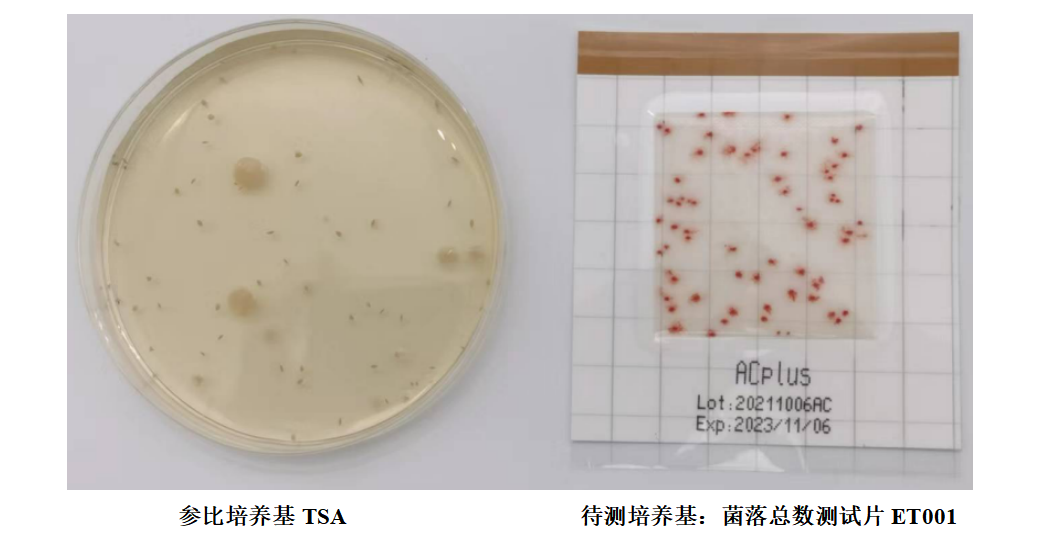
如果想了解到更多其他培養基驗收方法���,可關(guān)注“北京陸橋”公眾號�����。
